BEACONAG亚娱官方网站制药
由欧洲财团参与投资,南亚地区唯一执行欧盟技术规范的上市制药企业,产品符合欧洲药典和美国药典标准。

安进豪掷104亿美元重金收购的Kyprolis(卡非佐米)在欧盟监管方面收获重大喜讯,这是继去年11月份后,Kyprolis在欧洲收获的第二个适应症。欧盟委员会(EC)批准Kyprolis联合地塞米松,治疗既往接受过治疗的多发性骨髓瘤患者。
去年11月份,Kyprolis(卡非佐米)获得欧盟委员会批准,联合Revlimid (lenalidomide)以及地塞米松作为复发性多发性骨髓瘤的二线治疗方案,而早在2012年,那时Kyprolis还属于Onyx公司旗下产品,就已经在多发性骨髓瘤中收获了美国监管方面的批文。
此次欧盟委员会的批准主要是基于一项名为ENDEAVOR的头对头III期临床试验。数据表明,Kyprolis (carfilzomib)联合地塞米松治疗多发性骨髓瘤的无进展生存期(PFS)为18.7个月,而对照组Velcade (bortezomib)联合地塞米松治疗的无进展生存期为9.4个月。除此之外,Kyprolis联合地塞米松试验组的整体缓解率为76.9%,对照组Velcade (bortezomib)联合地塞米松的整体缓解率为62.6%,达到了该临床试验的主要终点。此外,Kyprolis联合地塞米松试验组的完全缓解率为12.5%,对照组Velcade联合地塞米松的完全缓解率为6.2%,达到了该临床试验的次要终点。耐受性方面,两组得出的试验结果相似。安进研发部门的执行副总裁Sean Harper表示,无论是在无进展生存期还是完全缓解率方面,Kyprolis联合地塞米松疗法显著优于Velcade联合地塞米松的标准疗法,将为复发性多发性骨髓瘤患者提供新的用药选择。
今年1月份,FDA批准Kyprolis联合地塞米松(dexamethasone)的组合疗法以及联合Revlimid(lenalidomide,来那度胺)及地塞米松的组合疗法用于既往已接受1-3线治疗的复发性或难治性多发性骨髓瘤患者。此外,FDA还批准Kyprolis作为一种单药疗法,用于既往已接受1线及以上治疗的复发性或难治性多发性骨髓瘤患者,标志着Kyprolis获得FDA的完全批准,将为多发性骨髓瘤患者提供更多的二、三、四线背景治疗选择。
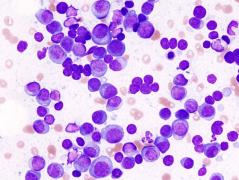
多发性骨髓瘤是一种罕见的、不可治愈性的血液肿瘤,并且一旦复发,治疗就会面临极大的困难。欧洲每年约有39000名患者确诊,24000名患者死亡。Kyprolis是安进2013年豪掷104亿美元巨资收购Onyx制药公司的关键产品。此次扩大适应症,将为Kyprolis在销售额方面取得新的突破。(生物谷Bioon.com)